1. Pengetahuan asas (jika anda ingin melihat bahagian eksperimen, sila pindahkan terus ke bahagian kedua)
Sebagai tindak balas derivatif PCR konvensional, PCR masa Nyata terutamanya memantau perubahan jumlah produk penguatan dalam setiap kitaran tindak balas penguatan PCR dalam masa nyata melalui perubahan isyarat pendarfluor, dan secara kuantitatif menganalisis templat permulaan melalui hubungan antara nilai ct dan lengkung standard .
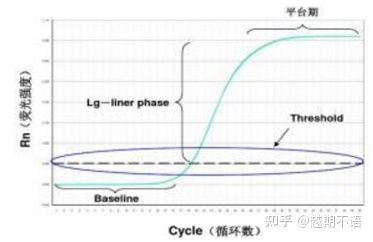
Data khusus RT-PCR ialahgaris dasar, ambang pendarfluordanNilai Ct.
| garis dasar: | Nilai pendarfluor kitaran ke-3-15 ialah garis dasar (garis dasar), yang disebabkan oleh ralat pengukuran sekali-sekala. |
| Ambang (ambang): | Merujuk kepada had pengesanan pendarfluor yang ditetapkan pada kedudukan yang sesuai dalam kawasan pertumbuhan eksponen lengkung amplifikasi, secara amnya 10 kali sisihan piawai garis dasar. |
| Nilai CT: | Ia adalah bilangan kitaran PCR apabila nilai pendarfluor dalam setiap tiub tindak balas mencapai ambang. Nilai Ct adalah berkadar songsang dengan jumlah templat awal. |
Kaedah pelabelan biasa untuk RT-PCR:
| kaedah | kelebihan | kelemahan | skop permohonan |
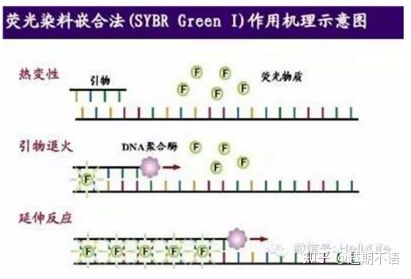
| SYBR GreenⅠ | Kebolehgunaan yang luas, sensitif, murah dan mudah | Keperluan primer adalah tinggi, terdedah kepada jalur tidak khusus | Ia sesuai untuk analisis kuantitatif pelbagai gen sasaran, penyelidikan tentang ekspresi gen, dan penyelidikan tentang haiwan dan tumbuhan rekombinan transgenik. |
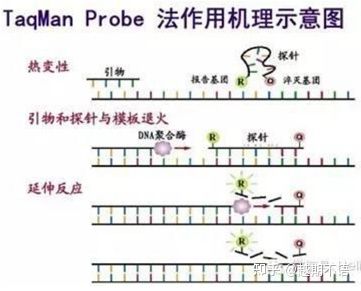
| TaqMan | Kekhususan yang baik dan kebolehulangan yang tinggi | Harganya tinggi dan hanya sesuai untuk matlamat tertentu. | Pengesanan patogen, penyelidikan gen rintangan dadah, penilaian keberkesanan ubat, diagnosis penyakit genetik. |
| suar molekul | Kekhususan tinggi, pendarfluor, latar belakang rendah | Harganya tinggi, ia hanya sesuai untuk tujuan tertentu, reka bentuknya sukar, dan harganya tinggi. | Analisis gen khusus, analisis SNP |
2. Langkah eksperimen
2.1 Mengenai kumpulan eksperimen- mesti ada beberapa telaga dalam kumpulan, dan mesti ada pengulangan biologi.
| ① | Kawalan kosong | Digunakan untuk mengesan status pertumbuhan sel dalam eksperimen |
| ② | SiRNA kawalan negatif (jujukan siRNA tidak spesifik) | Menunjukkan kekhususan tindakan RNAi.siRNA boleh mendorong tindak balas tekanan tidak spesifik pada kepekatan 200nM. |
| ③ | Kawalan Reagen Transfeksi | Kecualikan ketoksikan reagen pemindahan ke sel atau kesan pada ekspresi gen sasaran |
| ④ | siRNA terhadap gen sasaran | Tumbangkan ekspresi gen sasaran |
| ⑤ (pilihan) | siRNA positif | Digunakan untuk menyelesaikan masalah sistem eksperimen dan masalah operasi |
| ⑥ (pilihan) | siRNA kawalan pendarfluor | Kecekapan pemindahan sel boleh diperhatikan dengan mikroskop |
2.2 Prinsip reka bentuk primer
| Saiz serpihan diperkuat | Sebaiknya pada 100-150bp |
| Panjang Primer | 18-25bp |
| kandungan GC | 30%-70%, sebaik-baiknya 45%-55% |
| Nilai tm | 58-60 ℃ |
| Urutan | Elakkan T/C berterusan;A/G berterusan |
| 3 urutan akhir | Elakkan kaya GC atau kaya AT;pangkalan terminal adalah sebaik-baiknya G atau C;adalah yang terbaik untuk mengelakkan T |
| Pelengkap | Elakkan urutan pelengkap lebih daripada 3 asas dalam primer atau antara dua primer |
| Kekhususan | Gunakan carian letupan untuk mengesahkan kekhususan primer |
①SiRNA adalah khusus spesies, dan urutan spesies yang berbeza akan berbeza.
②SiRNA dibungkus dalam serbuk kering beku, yang boleh disimpan secara stabil selama 2-4 minggu pada suhu bilik.
2.3 Alat atau reagen yang perlu disediakan lebih awal
| Primer (rujukan dalaman) | Termasuk dua ke hadapan dan belakang |
| Primer (gen sasaran) | Termasuk dua ke hadapan dan belakang |
| Sasaran Si RNA (3 jalur) | Secara amnya, syarikat akan mensintesis 3 jalur, dan kemudian memilih salah satu daripada tiga oleh RT-PCR |
| Kit Transfeksi | Lipo2000 dsb. |
| Kit Pengekstrakan Pantas RNA | Untuk pengekstrakan RNA selepas pemindahan |
| Kit Transkripsi Terbalik Pantas | untuk sintesis cDNA |
| Kit Penguatan PCR | 2×Super SYBR Hijau Campuran Induk qPCR |
2.4 Berkenaan isu-isu yang perlu diberi perhatian dalam langkah-langkah eksperimen tertentu:
①proses pemindahan siRNA
1. Untuk penyaduran, anda boleh memilih plat 24-telaga, plat 12-telaga atau plat 6-telaga (purata kepekatan RNA yang dicadangkan dalam setiap telaga plat 24-telaga adalah kira-kira 100-300 ng/uL), dan ketumpatan transfeksi optimum sel adalah sehingga 60 %-80% atau lebih.
2. Langkah-langkah pemindahan dan keperluan khusus adalah mengikut arahan.
3. Selepas pemindahan, sampel boleh dikumpulkan dalam masa 24-72 jam untuk pengesanan mRNA (RT-PCR) atau pengesanan protein dalam masa 48-96 jam (WB)
② Proses pengekstrakan RNA
1. Mencegah pencemaran oleh enzim eksogen.Ia terutamanya termasuk memakai topeng dan sarung tangan dengan ketat;menggunakan petua pipet yang disterilkan dan tiub EP;air yang digunakan dalam eksperimen mestilah Bebas RNase.
2. Adalah disyorkan untuk melakukan dua kali seperti yang dicadangkan dalam kit pengekstrakan cepat, yang benar-benar akan meningkatkan ketulenan dan hasil.
3. Cecair sisa tidak boleh menyentuh lajur RNA.
③ Kuantifikasi RNA
Selepas RNA diekstrak, ia boleh dikira secara langsung dengan Nanodrop, dan bacaan minimum boleh serendah 10ng/ul.
④Proses transkripsi terbalik
1. Oleh kerana sensitiviti RT-qPCR yang tinggi, sekurang-kurangnya 3 telaga selari perlu dibuat untuk setiap sampel untuk mengelakkan Ct berikutnya daripada terlalu berbeza atau SD terlalu besar untuk analisis statistik.
2. Jangan beku dan cairkan adunan Master berulang kali.
3. Setiap tiub/lubang mesti diganti dengan hujung baru!Jangan gunakan hujung pipet yang sama secara berterusan untuk menambah sampel!
4. Filem yang dipasang pada plat 96-telaga selepas menambah sampel perlu dilicinkan dengan plat.Adalah lebih baik untuk mengempar sebelum meletakkannya pada mesin, supaya cecair pada dinding tiub boleh mengalir ke bawah dan mengeluarkan gelembung udara.
⑤Analisis lengkung biasa
| Tiada tempoh pertumbuhan logaritma | Mungkin kepekatan templat yang tinggi |
| Tiada nilai CT | Langkah yang salah untuk mengesan isyarat pendarfluor; degradasi primer atau probe - integritinya boleh dikesan oleh elektroforesis PAGE; jumlah templat yang tidak mencukupi; degradasi templat – mengelakkan kemasukan kekotoran dan pembekuan dan pencairan berulang dalam penyediaan sampel; |
| Ct>38 | Kecekapan amplifikasi rendah;Produk PCR terlalu panjang;pelbagai komponen tindak balas terdegradasi |
| Keluk penguatan linear | Probe mungkin sebahagiannya terdegradasi oleh kitaran beku-cair berulang atau pendedahan berpanjangan kepada cahaya |
| Perbezaan dalam lubang pendua sangat besar | Larutan tindak balas tidak cair sepenuhnya atau larutan tindak balas tidak bercampur;mandi terma instrumen PCR dicemari oleh bahan pendarfluor |
2.5 Mengenai analisis data
Analisis data qPCR boleh dibahagikan kepada kuantifikasi relatif dan kuantifikasi mutlak.Sebagai contoh, sel dalam kumpulan rawatan berbanding dengan sel dalam kumpulan kawalan,
Berapa kali mRNA gen X berubah, ini adalah kuantifikasi relatif;dalam bilangan sel tertentu, mRNA gen X
Berapa banyak salinan yang ada, ini adalah kuantiti mutlak.Biasanya yang paling kita gunakan dalam makmal ialah kaedah kuantitatif relatif.Biasanya,kaedah 2-ΔΔctpaling banyak digunakan dalam eksperimen , jadi hanya kaedah ini akan diperkenalkan secara terperinci di sini.
Kaedah 2-ΔΔct: Keputusan yang diperolehi ialah perbezaan dalam ekspresi gen sasaran dalam kumpulan eksperimen berbanding gen sasaran dalam kumpulan kawalan.Kecekapan penguatan kedua-dua gen sasaran dan gen rujukan dalaman adalah hampir 100%, dan sisihan relatif tidak boleh melebihi 5%.
Kaedah pengiraan adalah seperti berikut:
Kumpulan kawalan Δct = nilai ct gen sasaran dalam kumpulan kawalan – nilai ct gen rujukan dalaman dalam kumpulan kawalan
Δct kumpulan eksperimen = nilai ct gen sasaran dalam kumpulan eksperimen - nilai ct gen rujukan dalaman dalam kumpulan eksperimen
ΔΔct=Δct kumpulan eksperimen-Δct kumpulan kawalan
Akhir sekali, kirakan gandaan perbezaan dalam tahap ungkapan:
Tukar Lipatan=2-ΔΔct (sepadan dengan fungsi excel ialah POWER)
Produk Berkaitan:
Masa siaran: Mei-20-2023